- Autor Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:37.
- Viimati modifitseeritud 2025-06-01 07:36.
Peamine erinevus - alifaatsed vs aromaatsed süsivesinikud
Vaadakem kõigepe alt lühid alt, millised süsivesinikud räägivad erinevusest alifaatsete ja aromaatsete süsivesinike vahel. Süsivesinikud on orgaanilised ühendid, mis sisaldavad oma struktuuris süsiniku ja vesiniku aatomeid. Peamine erinevus alifaatsete ja aromaatsete süsivesinike vahel on see, et alifaatsed süsivesinikud ei sisalda konjugeeritud sidemete süsteemi, samas kui aromaatsed süsivesinikud sisaldavad konjugeeritud sidemete süsteemi. Neid mõlemaid molekule peetakse siiski orgaanilisteks ühenditeks.
Mis on alifaatsed süsivesinikud?
Alifaatsed süsivesinikud on orgaanilised molekulid, mis sisaldavad oma struktuuris süsiniku (C) ja vesiniku (H) aatomeid; sirgete, hargnenud ahelate või mittearomaatsete rõngastega. Alifaatsed süsivesinikud võib liigitada kolme põhirühma; alkaanid, alkeenid ja alküünid.
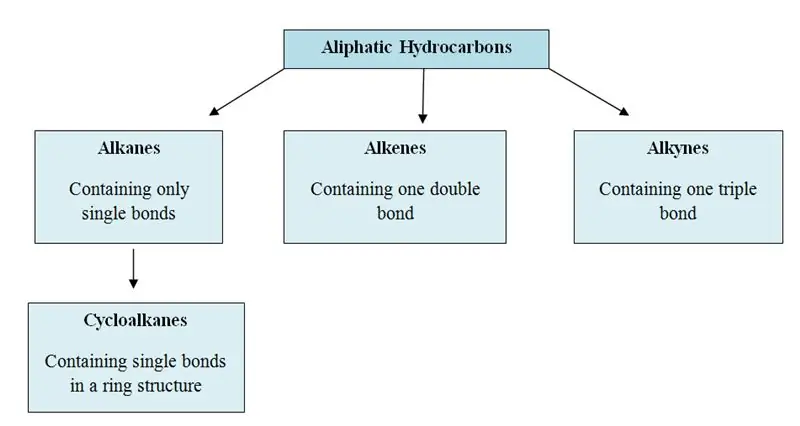
Mis on aromaatsed süsivesinikud?
Aromaatseid süsivesinikke tuntakse mõnikord kui "areenid" või "arüülsüsivesinikud". Enamiku aromaatsete süsivesinike struktuuris on benseenitsükkel; kuid on ka mittebenseeni aromaatseid süsivesinikke, mida nimetatakse heteroareenideks ja mis järgivad "Huckle'i reeglit" (tsüklilistel tsüklitel, mis järgivad Huckle'i reeglit, on 4n+2 arv π-elektrone; kus n=0, 1, 2, 3, 4, 5, 6). Mõnedel aromaatsetel süsivesinikel on rohkem kui üks ring; neid nimetatakse polütsüklilisteks aromaatseteks süsivesinikeks.
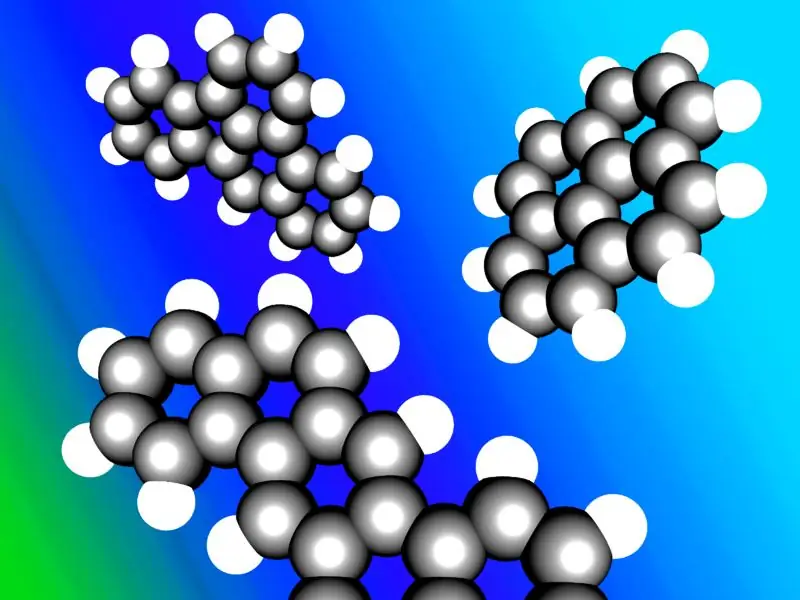
Tüüpiliste polütsükliliste aromaatsete süsivesinike illustratsioon.
Mis vahe on alifaatsetel ja aromaatsetel süsivesinikel?
Alifaatsete ja aromaatsete süsivesinike struktuur
Alifaatsed süsivesinikud: nende struktuuris on sirged ahelad, hargnenud ahelad või mittearomaatsed rõngad. Selles rühmas on nii küllastunud kui ka küllastumata süsivesinikke. Alkaanid on küllastunud süsivesinikud, alkeenid ja alküünid on küllastumata süsivesinikud.
Sirged ketid:
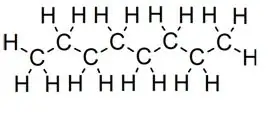
Oktaaniarv
Kaubamärgiga ketid:
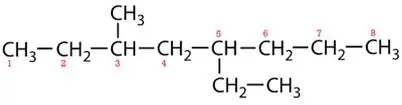
5-etüül-3-metüüloktaan

2-metüül-3-pentent
Mittearomaatsed rõngad:
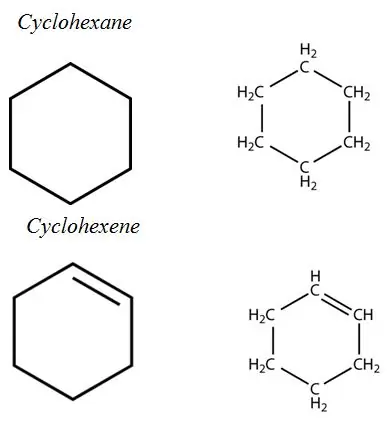
Aromaatsed süsivesinikud: aromaatsete süsivesinike struktuuris on aromaatne tsüklisüsteem. Need on kõik küllastumata süsivesinikud, kuid konjugeeritud sidemete süsteemi tõttu suhteliselt stabiilsed.
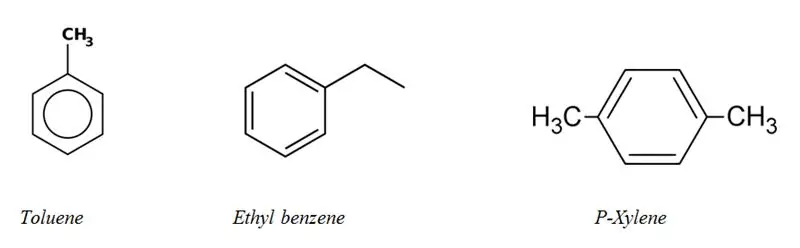
Alifaatsete ja aromaatsete süsivesinike kategooriad
Alifaatsed süsivesinikud:
Alifaatsetes süsivesinikes on kolm peamist rühma; alkaanid, alkeenid ja alküünid. Neid tuntakse ka allüülsüsivesinikena.
Alkaanid: alkaanides on süsiniku- ja vesinikuaatomid omavahel seotud üksiksidemetega. Neil ei ole mitut võlakirja. Alkaanid moodustavad ringstruktuure, neid nimetatakse tsükloalkaanideks.
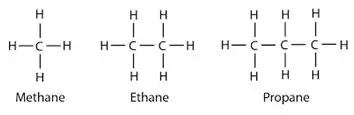
Alkeenid: see rühm sisaldab nii üksik- kui ka kaksiksidemeid süsinikuaatomite vahel. Vesiniku- ja süsinikuaatomid moodustavad alati üksiksidemeid.
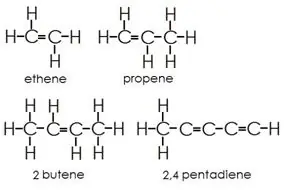
Alküünid: alküünidel on lisaks üksiksidemetele ka kolmiksidemed süsinikuaatomite vahel.
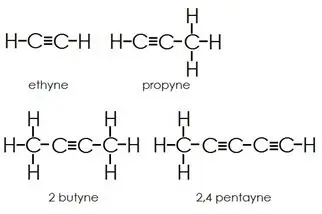
Aromaatsed süsivesinikud:
Enamiku aromaatsete süsivesinike struktuuris on vähem alt üks benseenitsükkel. Kuid mitte-benseeni aromaatseid süsivesinikke on vähe, neid nimetatakse "heteroareenideks". Aromaatseid süsivesinikke nimetatakse arüülsüsivesinikeks.
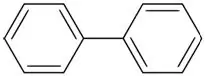
Bifenüül (kahe benseenitsükliga aromaatne süsivesinik)
Alifaatsete ja aromaatsete süsivesinike sidumismuster
Alifaatsed süsivesinikud:
Alifaatsetes süsivesinikes; üksik-, kaksiks- või kolmiksidemed võivad eksisteerida kõikjal molekulis. Mõnikord võib ühe molekulaarse valemi jaoks olla mitu struktuuri, muutes mitme sideme asendit. Nendel molekulidel on lokaliseeritud elektronsüsteem.
Aromaatsed süsivesinikud:
Aromaatsetes süsivesinikes on neil alternatiivne üksik- ja kaksiksideme süsteem, et moodustada konjugeeritud sidemete süsteem mõne elektroni ümberpaigutamiseks. (Delokaliseeritud elektronid võivad liikuda ühest sidemest teise).
Alifaatsete ja aromaatsete süsivesinike reaktsioonid
Alifaatsed süsivesinikud:
Küllastunud süsivesinikud läbivad asendusreaktsioonid; küllastumata süsivesinikud saavutavad stabiilsuse liitumisreaktsiooniga. Kuid mõned reaktsioonid toimuvad kontrollitud tingimustes ilma mitut sidet purustamata.
Aromaatsed süsivesinikud:
Aromaatsed süsivesinikud on küllastumata, kuid neil on stabiilne konjugeeritud elektronsüsteem, nii et nad on pigem vastuvõtlikud asendusreaktsioonidele kui liitumisreaktsioonidele.
Pilt: Inductiveload "Polycyclic Aromatic Carbons" - üleslaadija enda töö, Accelrys DS Visualizer. (avalik domeen) Commonsi kaudu






